El sistema® de Braquiterapia Electrónica (eBx®) y Radioterapia Intraoperatoria (RIO) Xoft® Axxent®, aprobado por la FDA y con marcado CE, está autorizado en un número creciente de países para el tratamiento de los cánceres de mama en etapa temprana, piel no melanoma y ginecológicos. Entre otras indicaciones, actualmente se está investigando su aplicación para el tratamiento de tumores cerebrales y, en concreto, para la recidiva de glioblastoma donde se han obtenido resultados preliminares muy prometedores.
El sistema Xoft® Axxent® (eBx®) utiliza tecnología de braquiterapia electrónica de vanguardia. La braquiterapia permite dirigir la dosis de radiación al tamaño y la forma del área cancerosa, evitando el daño en los tejidos y órganos sanos circundantes. El término braquiterapia “electrónica” hace referencia a que la fuente de rayos X miniaturizada es libre de isótopos, por lo que requiere un blindaje mínimo, a la vez que administra una radiación de alta dosis y baja energía.
La Radioterapia Intraoperatoria (RIO) utilizando el sistema Xoft® consiste en la administración de alta dosis de radiación en el mismo lecho tumoral tras la cirugía de resección o extirpación del tumor. Sus ventajas son la rápida implementación del procedimiento, el flujo de trabajo mínimo y, además, permite la planificación de la radioterapia y la monitorización intraoperatoria. De esta manera, una única sesión de braquiterapia electrónica intraoperatoria distribuye una dosis equivalente a varias sesiones de radioterapia externa fraccionada. Esto permite minimizar la dosis de radiación que alcanza al tejido sano adyacente.
El sistema Xoft® ya se emplea para el tratamiento de los cánceres de mama1,2, piel no melanoma3 y ginecológicos4. Actualmente se están realizando estudios para aplicar este sistema de braquiterapia electrónica en cerebro, páncreas, colorrectal y próstata. En este artículo nos centraremos en los estudios en curso en instituciones de primer orden a nivel mundial para el tratamiento de distintos tipos de tumores cerebrales, con un foco especial en el tratamiento de la recurrencia de glioblastoma.
Tratamiento de glioblastoma con el sistema Xoft®
En 2020 se reportaron mundialmente 300 000 casos de cánceres del sistema nervioso central (SNS)5. De acuerdo al informe de CBTRUS, el más común de los tumores malignos del SNS es el glioblastoma, que corresponde a un 48.3% del total de cánceres del sistema nervioso. Además, la supervivencia del glioblastoma es muy baja, solo un 6.8% de los pacientes de Estados Unidos viven 5 años tras el diagnóstico6.
El tratamiento estándar para el glioblastoma es la cirugía de extirpación del tumor, que no es de por sí curativa, sino que requiere de tratamiento adyuvante postoperatorio con radioterapia externa y quimioterapia con temozolomida. Este tratamiento adyuvante debe comenzarse a las 4-6 semanas de la cirugía, siempre dependiendo del perfil histológico y genético molecular del tumor7, con el fin de evitar recaídas tempranas.
Sin embargo, a pesar del tratamiento, la supervivencia de los pacientes con glioblastoma no ha mejorado considerablemente en los últimos 50 años, produciéndose la muerte de la mayoría a los 12-15 meses. Esto se debe a que el glioblastoma es un tumor muy resistente a la radio y quimioterapia. Además, se conoce que los corticoesteroides, la temozolomida y la propia radiación son inmunosupresores que pueden comprometer la supervivencia de los pacientes8. En el caso de la radiación externa, esta podría incluso modificar el ambiente de los axones, induciendo un aumento en la proporción de células cancerosas.
A pesar de estos datos, se ha registrado una mejora del 10% de la supervivencia a largo plazo de los pacientes con glioblastoma. Dicha mejora proviene de los avances en la cirugía que han permitido una mayor resección del tumor9. Cuando el volumen de tumor remanente es menor de 2.5 centímetros cúbicos se obtiene un pronóstico más favorable10. De hecho, una resección parcial podría conllevar edema y hemorragias cerebrales, así como un rápido recrecimiento del tumor.
Se están investigando otros tratamientos como la inmunoterapia y la terapia dirigida, pero de momento no han resultado efectivos o solo a nivel sintomático. Además, el panorama se complica porque la mayoría de casos de glioblastoma recidivan a los 6-7 meses del término del tratamiento adyuvante, por lo que la reaparición del glioblastoma se considera prácticamente inevitable. El problema es que actualmente no se dispone de un tratamiento para la recurrencia del glioblastoma. Por un lado, no hay evidencia de que repetir la cirugía de resección tenga resultados más favorables que administrar únicamente radio y/o quimioterapia, aunque sí resulta beneficioso en los pacientes que presentan síntomas derivados del volumen tumoral7. Por otro lado, la radioterapia externa postoperatoria está limitada de forma frecuente por el alto riesgo de complicaciones derivadas de la radiación como, por ejemplo, radionecrosis. Por eso, los médicos especialistas se plantean optimizar la cirugía con la aplicación de otras técnicas como la RIO o introduciendo medicamentos quimioterapéuticos en la cavidad de resección del tumor.
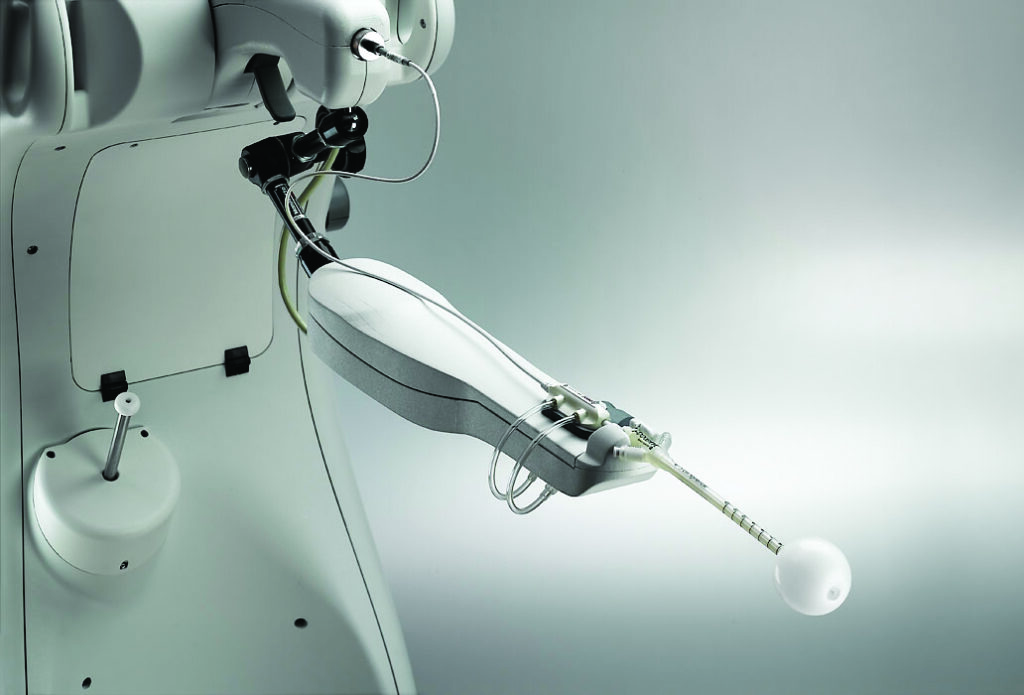
Estudio de los beneficios clínicos del sistema Xoft® para la recidiva de glioblastoma
En realidad, la experimentación clínica con RIO en cerebro comienza en los años 1970 en Japón. A lo largo de los años, se ha refinado el procedimiento usando, por ejemplo, aplicadores sólidos o de balón esférico que permiten ajustarse a la irregularidad de los lechos tumorales consiguiendo una administración más precisa de la dosis de radiación y evitando irradiar el tejido sano circundante. La investigación en RIO para el tratamiento de tumores cerebrales perdió empuje con otros avances como la introducción de la temozolomida, el uso de resonancia magnética intraoperatoria y, sobre todo, con la resección quirúrgica guiada por fluorescencia7. Teniendo en cuenta que no se dispone de una terapia que impida las recidivas ni un tratamiento estándar para los casos de glioblastoma recurrente, urge estudiar nuevos enfoques entre los que la RIO resulta una aproximación prometedora.
El European Medical Center (EMC) de Moscú es una de las mayores clínicas privadas de Rusia, siendo líder internacional en oncología. En EMC disponen de una amplia experiencia en el uso de Xoft® para cánceres de mama, piel no melanoma y ginecológicos. Desde 2016 se encuentran estudiando el tratamiento de la recidiva del glioblastoma repitiendo la cirugía de resección del tumor y administrando RIO con el sistema Xoft®. El estudio piloto realizado entre 2016-2019 contó con 30 pacientes, 15 pertenecientes al grupo control y la otra mitad al grupo experimental, procurándose que ambos grupos fueran homogéneos en cuanto a las características de los pacientes. Al grupo control se le aplicó la segunda cirugía de resección del tumor proporcionándoles tratamiento postoperatorio adyuvante de radio y quimioterapia en el Meshalkin Medical Research Center de Novosibirsk, Rusia. El grupo experimental, en cambio, después de la cirugía recibió únicamente RIO con el sistema Xoft®. Una de las ventajas de Xoft® es que su aplicador de balón permite un mayor ajuste y adherencia a la cavidad tumoral, lo que se puede confirmar mediante ultrasonido intraoperatorio. De esta forma, se asegura que la administración de la dosis de radiación tiene lugar por la superficie del balón, permitiendo esterilizar la cavidad del tumor y disminuyendo la probabilidad de nuevas recidivas. Este procedimiento es mínimamente invasivo, generalmente se lleva a cabo en 20 minutos, tiene un perfil de toxicidad generado e incluso la adherencia del balón a la cavidad tumoral es capaz de detener hemorragias.
De acuerdo a los resultados presentados en varios congresos11,12, la mediana de supervivencia global del grupo experimental fue de 27 meses con respecto a los 21 del grupo control. El intervalo de supervivencia libre de progresión, es decir, los pacientes que tras un período de tiempo definido se mantuvieron sin empeoramiento, fue de entre 3.5 y 39 meses para el grupo experimental, mientras que para el grupo control se obtuvo de 2 a 20 meses. Estas significativas mejoras en la supervivencia estadística fueron incrementadas para el subgrupo de pacientes en los que la repetición de la cirugía había conseguido una mayor resección del tumor, dejando un volumen tumoral remanente igual o menor a 2.5 centímetros cúbicos.
Además, se observó que en el grupo control se produjo la reaparición del glioblastoma en todos los 15 pacientes, mientras que en el grupo experimental hubo 10 recaídas. En cuanto a las complicaciones derivadas de la administración de RIO, no hubo ningún caso de infección y solo 2 pacientes presentaron radionecrosis. En comparación, en el grupo de control hubo 4 pacientes con radionecrosis y otros 2 que sufrieron hemorragias. Por último, en septiembre de 2019, nueve pacientes del grupo experimental seguían vivos mientras que todos los del grupo control habían fallecido.
Por supuesto, estos resultados preliminares requieren confirmación mediante nuevos estudios multicentro, que incluyan tanto glioblastomas primarios como recidivas.
Aplicación del sistema Xoft® en otros tipos de tumores cerebrales
En el EMC de Moscú también han comenzado a aplicar RIO con el sistema Xoft® en otros tumores cerebrales, de momento, en 6 pacientes con gliomas de alto grado y 4 pacientes con diferentes tipos de metástasis.
Otros estudios en curso son el del James Graham Brown Cancer Center de la Universidad de Louisville y el ensayo GLIOX. El primer caso consiste en un ensayo clínico de RIO con Xoft® en pacientes con metástasis cerebrales que lleva en marcha desde febrero de 202013. El ensayo GLIOX, por otra parte, se trata de un estudio de fase II para pacientes con recidiva de glioblastoma, que serán tratados con cirugía de resección máxima del tumor y con RIO por medio de la braquiterapia electrónica de Xoft Axxent, además de con bevacizumab14.
Igualmente se considera que el sistema Xoft® podría tener aplicación para recidivas de gliomas anaplásicos, potenciales meningiomas y diferentes metástasis cerebrales.
La radioterapia intraoperatoria para tumores cerebrales por medio del sistema Xoft® de braquiterapia electrónica podría mejorar la calidad de vida de los pacientes con pronóstico grave. La RIO con braquiterapia electrónica tiene el potencial de prolongar la vida de los pacientes con diversos tipos de cáncer, incluidos los tumores cerebrales metastásicos y el glioblastoma.
Si desea más información de los estudios en curso de Xoft® para la aplicación de su sistema de braquiterapia electrónica en distintos tumores cerebrales puede contactarnos en el siguiente enlace.
Referencias
1. Schwartzberg, B. S. et al. Application of 21-gene recurrence score results and ASTRO suitability criteria in breast cancer patients treated with intraoperative radiation therapy (IORT). Am. J. Surg. 216, 689–693 (2018).
2. Silverstein, M. J. et al. Intraoperative Radiation Therapy (IORT): A Series of 1000 Tumors. Ann. Surg. Oncol. 25, 2987–2993 (2018).
3. Patel, R. et al. Comparison of electronic brachytherapy and Mohs micrographic surgery for the treatment of early-stage non-melanoma skin cancer: a matched pair cohort study. J. Contemp. Brachytherapy 9, (2017).
4. Lozares-Cordero, S. et al. Postoperative endometrial cancer treatments with electronic brachytherapy source. J. Radiother. Pract. 18, 16–20 (2019).
5. International Agency for Research on Cancer. Globocan Cancer Incidence and Mortality Worldwide in 2018. (2021).
6. Ostrom, Q. T. et al. CBTRUS Statistical Report: Primary Brain and Other Central Nervous System Tumors Diagnosed in the United States in 2012-2016. Neuro. Oncol. 21, V1–V100 (2019).
7. Krivoshapkin, A. et al. Repeat Resection and Intraoperative Radiotherapy for Malignant Gliomas of the Brain: A History and Review of Current Techniques. World Neurosurg. 132, 356–362 (2019).
8. Grossman, S. A. et al. Immunosuppression in Patients with High-Grade Gliomas Treated with Radiation and Temozolomide. Clin. Cancer Res. (2011) doi:10.1158/1078-0432.CCR-11-0774.
9. Brawanski, A., Acerbi, F., Nakaji, P., Cohen-Gadol, A. & Schebesch, K. M. Poor man-rich man fluorescence. Is this really the problem? Acta Neurochir. (Wien). 157, 1959–1961 (2015).
10. Krivoshapkin, A. L. et al. Automated Volumetric Analysis of Postoperative Magnetic Resonance Imaging Predicts Survival in Patients with Glioblastoma. World Neurosurg. 126, e1510–e1517 (2019).
11. Gaytan, A. et al. Recurrent Glioblastoma Management With Maximal Safe Resection And Intraoperative Balloon Electronic Brachytherapy: Two Centers Study. in AANS (2021).
12. Salim, N. et al. Intra-operative radiation therapy as salvage treatment option for recurrent glioblastoma multiforme. J. Clin. Oncol. 38, 2535–2535 (2020).
13. Gaytan, A. Four-year experience of maximal safe resection with intraoperative balloon electronic brachytherapy for recurrent glioblastoma. in EANS (2020).
14. University of Louisville. Study of Intraoperative Radiotherapy for Patients With Large Brain Metastases Treated With Neurosurgical Resection. ClinicalTrials.gov.
15. Xoft. Recurrent GBM Treated With Neurosurgical Resection and IORT Using the Xoft Axxent eBx System and Bevacizumab. ClinicalTrials.gov.
