La física médica continúa como protagonista en la cuarta entrega de la serie de Hipertermia oncológica: ¿cuál es el camino hacia el tratamiento de calidad?. Estamos analizando los aspectos necesarios de esta terapia, entre ellos, cómo el camino hacia el tratamiento de calidad pasa por asimilar el flujo de trabajo de la hipertermia oncológica al de la radioterapia.
Esta serie de artículos proviene del webinar realizado en colaboración con la Sociedad Española de Física Médica (SEFM).
La hipertermia oncológica es una terapia adyuvante de la radioterapia y/o quimioterapia. Consiste en el calentamiento de los tumores entre 39-45 °C durante una hora. El objetivo es aumentar la efectividad del tratamiento primario[1].
En el primer artículo de esta serie se presentaron los mecanismos de acción y los aspectos físicos más relevantes de la terapia (sobre todo la temperatura alcanzada en el tumor[2] y el intervalo de tiempo entre la hipertermia y la radioterapia[3]). También se trató de las dos tecnologías más comunes en el mercado: capacitiva y radiativa.
El segundo artículo expuso las diferencias de las tecnologías por medio de las simulaciones numéricas de Kok et al.[4], [5] en distintas condiciones de hipertermia profunda y superficial.
El tercer artículo trató de las directrices de control de calidad de la ESHO (European Society for Hyperthermic Oncology) para hipertermia superficial[6], [7] e hipertermia profunda[8], [9].
En el cuarto artículo seguimos con la Física médica. En esta ocasión, el camino hacia el tratamiento de calidad pasa por asimilar el flujo de trabajo al de la radioterapia.
Los sistemas ALBA de Med-Logix, ALBA 4D de hipertermia profunda y ALBA ON 4000D de hipertermia superficial y semiprofunda, permiten adecuarse a un flujo de trabajo semejante al de la radioterapia para optimizar la terapia adyuvante.
ALBA 4D es el sistema de hipertermia profunda conformada. Sus cuatro antenas en fase trabajan a 70 MHz, irradiando cuatro haces. Los haces se modulan de forma independiente en fase y amplitud. Esto permite la colimación electromagnética automática de los cuatro haces de radiofrecuencia gracias a la superposición constructiva. Se enfoca la energía sobre el objetivo a cualquier profundidad y localización en pelvis, abdomen y extremidades.
ALBA ON 4000D es el sistema de hipertermia superficial y semiprofunda. La unidad funciona a una frecuencia fija de 434 MHz. Está equipada con cuatro aplicadores de diferentes tamaños de microstrip (tecnología CCMA): ALFA, BETA, GAMMA y DELTA. La superficie con radio de curvatura fijo y la frecuencia de trabajo de 434 MHz permiten calentar con eficacia lesiones superficiales de hasta unos 4 ± 0,5 cm de profundidad. Esta profundidad posibilita el tratamiento de lesiones superficiales y muchas lesiones semiprofundas.
Física médica: flujo de trabajo de la hipertermia oncológica
1. Planificación y simulación de hipertermia oncológica (PLAN2heat)
La planificación es necesaria en la radioterapia. De la misma manera, la planificación de la hipertermia ayuda con diversos aspectos del tratamiento. Por ejemplo, en hipertermia profunda con las configuraciones de fase adecuadas, análisis de la capacidad de calentamiento, supresión de puntos calientes. En hipertermia superficial con la selección del aplicador y evaluación de la cobertura del objetivo y la profundidad de calentamiento.
Además, los físicos médicos disponen en la actualidad de herramientas que les permiten realizar de forma fácil y efectiva los planes de hipertermia radiativa (ya sea superficial o profunda). Así confirman la dosis térmica óptima en el objetivo.
PLAN2heat (P2h) es el sistema de planificación del tratamiento de hipertermia de Med-Logix, con simulación 3D adaptativa. Es un codesarrollo con Amsterdam UMC y ahora mismo su uso se limita al ámbito de la investigación. Es decir, no se puede evaluar la dosimetría clínica con PLAN2heat. En todo caso se requiere que facultativos y radiofísicos hospitalarios continúen midiendo la temperatura de forma intraluminal o mínimamente invasiva o superficial. El fin es asegurar la administración de dosis térmica según las directrices de control de calidad de la ESHO (European Society Hyperthermia Oncology)[6], [8], [10].
No obstante, P2h puede predecir con exactitud la distribución de temperaturas y los potenciales puntos calientes. El marcado CE de PLAN2heat está en camino y se espera en este año 2026.
P2h es el primer software de simulación de hipertermia que se ha diseñado con integración en el dominio DICOM. Por tanto, facilita las decisiones clínicas, contribuyendo a mantener y mejorar la calidad del tratamiento[11].
PLAN2heat permite simulaciones de temperatura de pacientes con tumores a múltiples profundidades (superficiales, semiprofundos y profundos). En P2h se modela la configuración en fase del equipo ALBA 4D de hipertermia profunda y también los cuatro aplicadores de ALBA ON 4000D para tumores multiprofundos[12].
El flujo de trabajo de P2h da soporte a planes de hipertermia profunda (con ALBA 4D) o hipertermia superficial y semiprofunda (ALBA ON 4000D).
En el caso de ALBA 4D, se requiere una TC del paciente con el bolus de agua y sonda de temperatura. Así, se replican las condiciones realistas de tratamiento. Se importan los archivos DICOM (CT y RT STRUCT) y PLAN2heat realiza la segmentación automática de las unidades Hounsfield (UH) de la TC.
En el caso de ALBA ON 4000D, no se necesita una TC específica de hipertermia. Con este sistema, también se importan los archivos DICOM. A continuación, P2h realiza la segmentación automática según las UH de la TC.
En ambos casos, el planificador puede reconocer la grasa, hueso, músculo y aire a partir de las unidades Hounsfield. P2h contornea el GTV/PTV y órganos de riesgo o bien los importa del planificador. Además, delimita y elimina los artefactos.
Cálculo de dosis
En la construcción de un algoritmo de cálculo de dosis semejante a la radioterapia, se necesita una caracterización realista de las antenas y de la radiación electromagnética (potencia, frecuencia, fase, etc.).
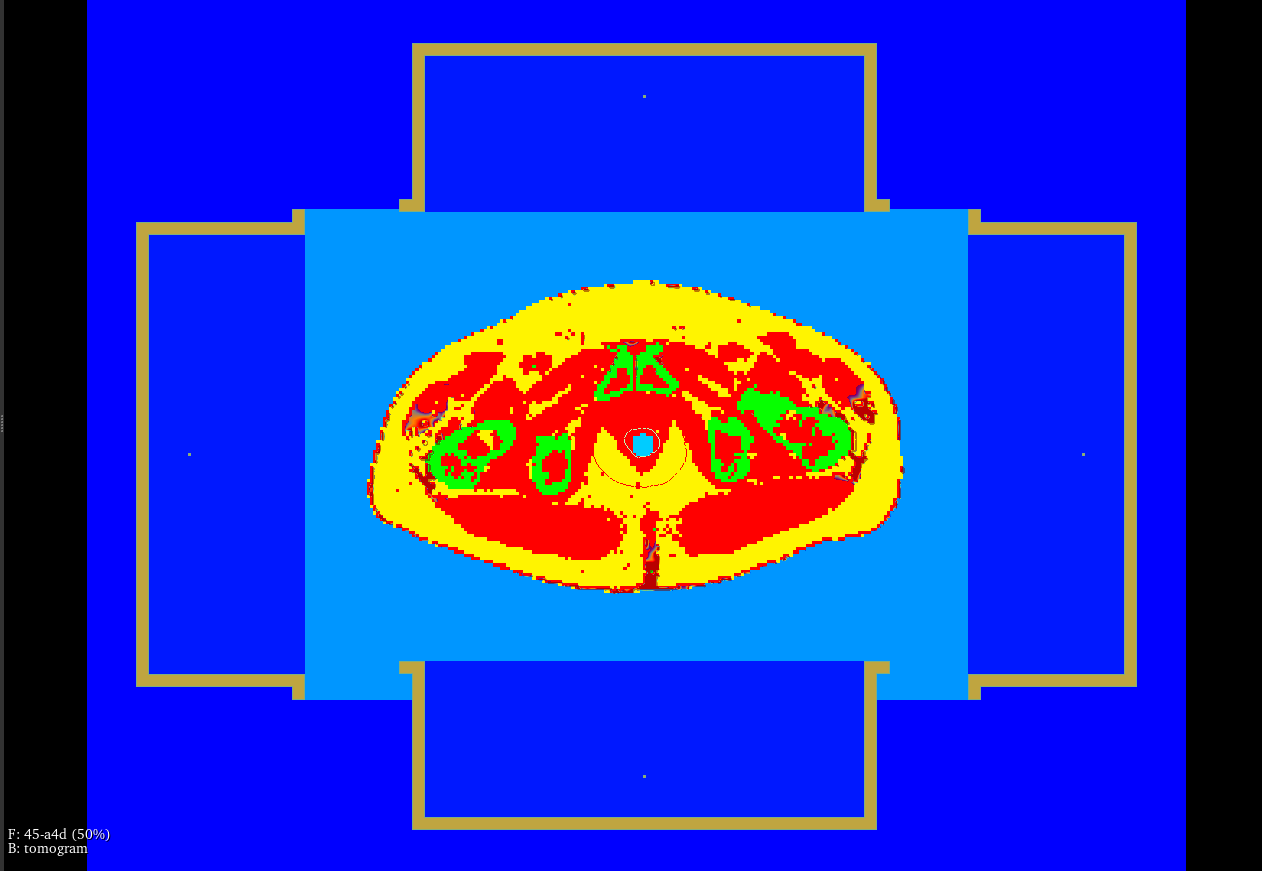
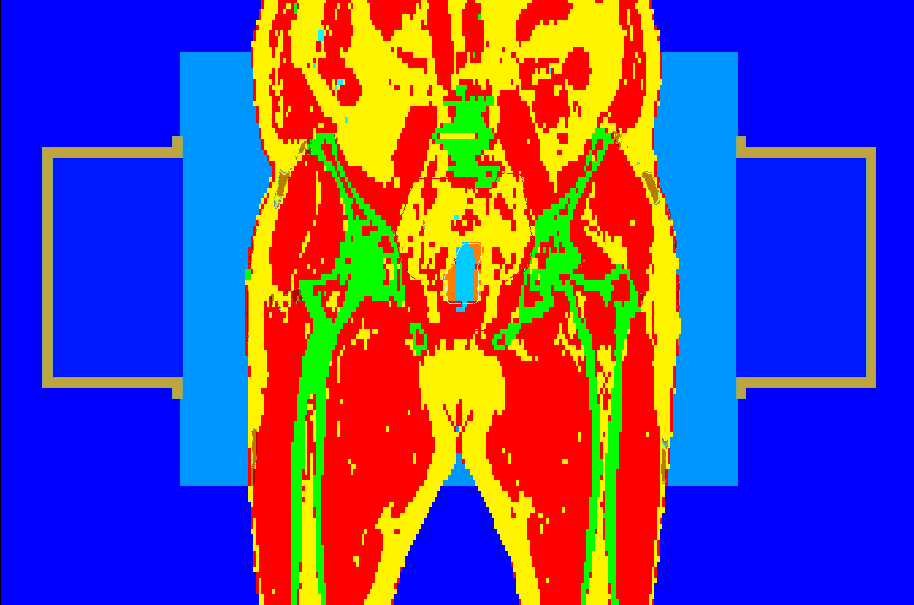
Las estrategias de cálculo incluyen SAR (energía del campo electromagnético depositada por unidad de masa) y las distribuciones de temperatura. SAR depende de las características de la radiación y del tejido. Las distribuciones de temperatura se calculan con la absorción de energía electromagnética por los distintos tejidos y con la perfusión. Para ello, se considera el calor específico del medio, posibles transmisiones, comportamientos fisiológicos, etc. A pesar de la complejidad que supone, se pueden emplear modelos disponibles en la bibliografía.
Una vez se reconocen los tipos de tejido a través de las unidades Hounsfield de la TC, PLAN2heat asigna las propiedades dieléctricas y térmicas específicas de los tejidos. Estas propiedades se extraen de la literatura científica y se almacenan en una base de datos dentro del planificador (TPS).
En P2h, el cálculo de la distribución del campo electromagnético se realiza con las ecuaciones dinámicas de Maxwell por cálculo de diferencias finitas (FDTD) por cada vóxel. La temperatura se determina resolviendo la ecuación de Pennes[4].
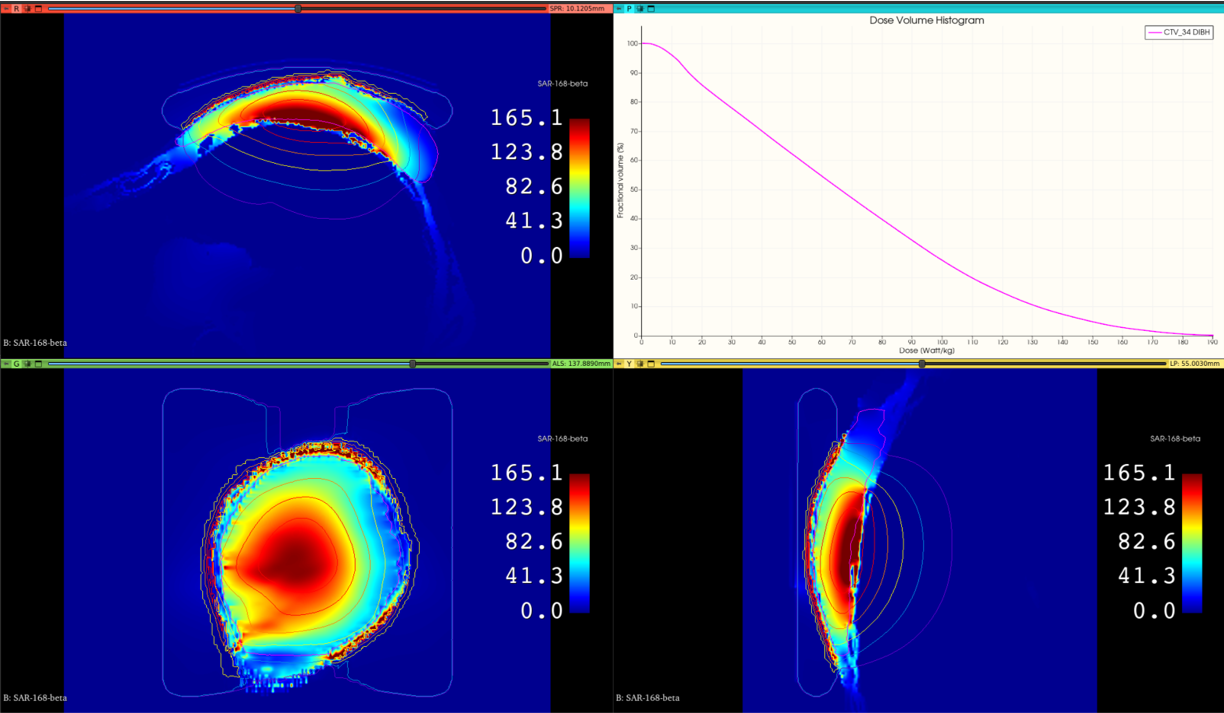
En el sistema ALBA 4D, PLAN2heat carga las antenas. Su posicionamiento se define por un punto (el centro del array), que se corresponde con el centro del paciente según el isocentro. A partir de todos estos datos, P2h genera un modelo en menos de 2 minutos.
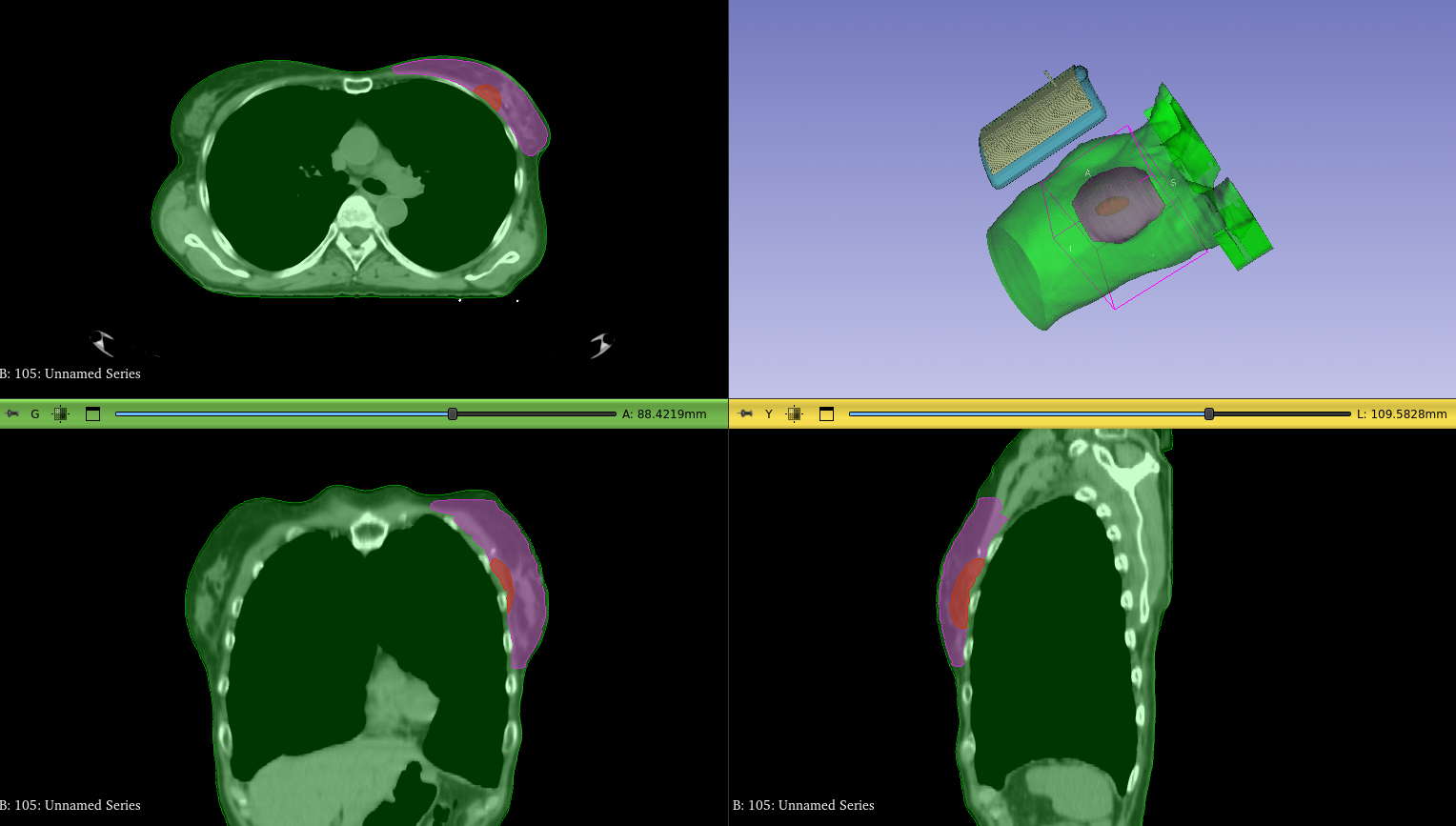
En ALBA ON 4000D, se importa el modelo del equipo con el modelado de las antenas que permite su posicionamiento. El tiempo de cálculo de posición es también menor de 2 minutos. PLAN2heat rellena de modo automático el hueco antena-paciente con las propiedades dieléctricas y las condiciones térmicas del bolus. De esta manera, se genera el modelo en el que la antena, tal como la ha posicionado el usuario, se inserta en el modelo final. En último lugar, se lleva a cabo la simulación que resulta en el mapa 3D de temperatura y de SAR. Se obtiene así el equivalente a los histogramas dosis-volumen (histogramas temperatura-volumen).
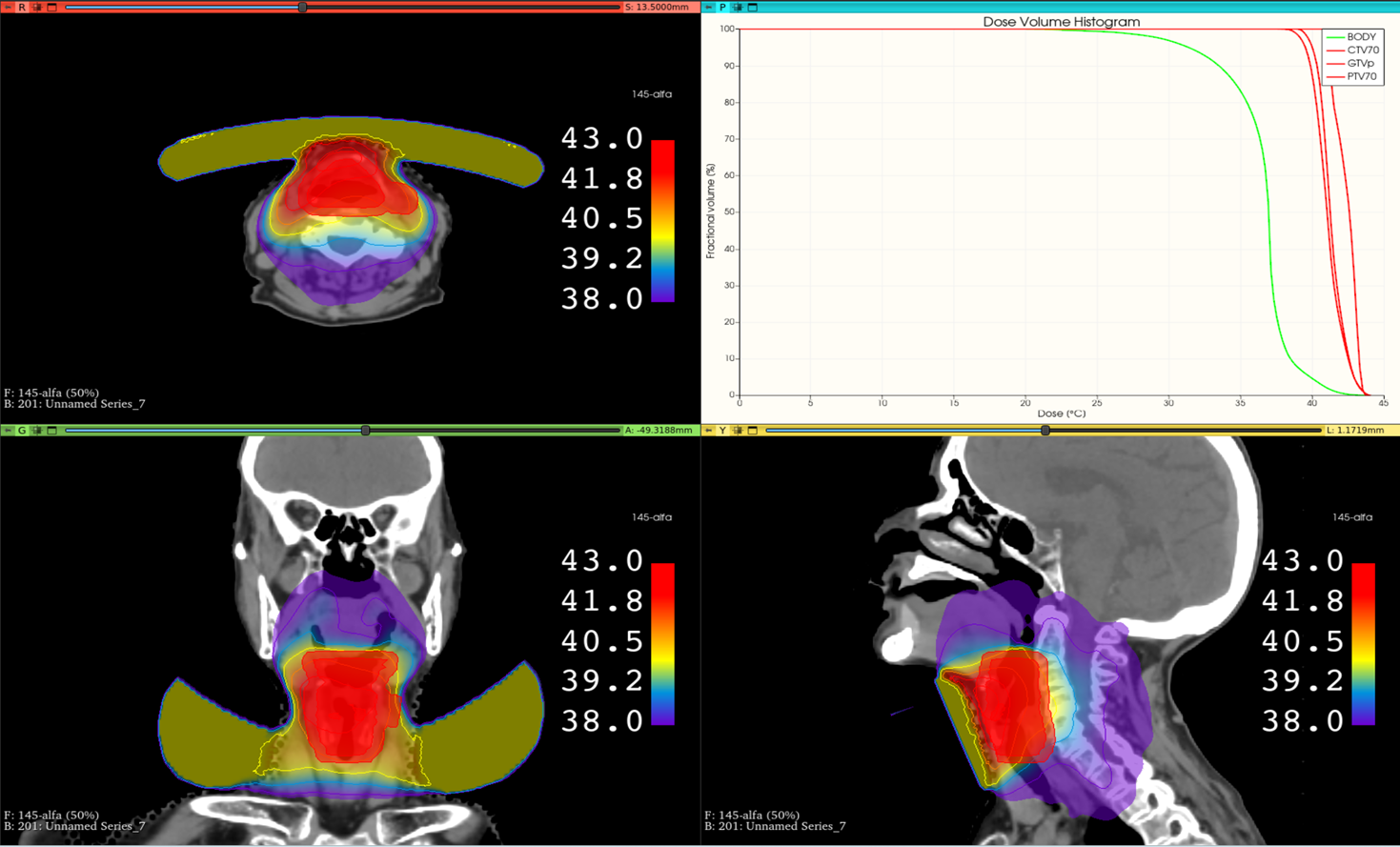
Por otra parte, se está trabajando en la combinación del mapa de dosis de radiación con el de temperatura y SAR de la hipertermia para obtener un mapa de dosis equivalente. En esta línea, la empresa RaySearch Laboratories, junto con Med-Logix y Amsterdam UMC, están desarrollando la planificación conjunta de termorradioterapia[13]. La cuantificación del efecto combinado de las terapias se calcula con la dosis equivalente de radiación en fracciones de 2 Gy (EQD2). Esta refleja la potenciación del efecto terapéutico y cómo los parámetros modificados de radio sensibilización pueden aumentar la dosis de radiación. En el estudio de Öden et al.[13] se propone un nuevo esquema de planificación de termorradioterapia con optimización vóxel a vóxel de EQD2.
2. Configuración y posicionamiento: easyPLAN y OPTIX
Similar a la radioterapia, lo deseable en hipertermia es el rigor en el posicionamiento, permitiendo el ajuste de parámetros según la simulación.
La propuesta de Med-Logix para los sistemas ALBA es el software de planificación geométrica easyPLAN, con marcado CE. easyPLAN facilita el flujo de trabajo y la transferencia de datos específicos del paciente en la configuración del tratamiento.
En ALBA 4D, easyPLAN proporciona sugerencias de la configuración de fase para la colimación de los cuatro haces de radiofrecuencia. También en cuanto al posicionamiento geométrico de las sondas de temperatura y su clasificación según la posición con respecto al objetivo y el tejido normal. Los cálculos de configuración de fase se exportan de manera automática a la consola de ALBA 4D.
easyPLAN dispone de un sistema de posicionamiento láser basado en señales anatómicas y de toda la parametrización de la máquina.
El equipo ALBA 4D tiene integrado un sistema láser que se inspira en los aceleradores lineales. Este posibilita el posicionamiento preciso del paciente por medio de tres láseres de alineamiento. Así, facilita la reproducibilidad del posicionamiento antenas/paciente en todos los tratamientos, además de la colimación de la configuración antenas/paciente con easyPLAN y PLAN2heat.
Con respecto a ALBA ON 4000D, la selección del aplicador depende del tamaño del tumor y su posición anatómica. En el anterior artículo de esta serie ya presentamos la guía óptica OPTIX de Med-Logix. OPTIX permite simplificar y acelerar el posicionamiento de los aplicadores del sistema con exactitud y repetibilidad entre sesiones.
Como PLAN2heat incorpora OPTIX, una vez terminada la simulación, se reenvía toda la información a la plataforma. En OPTIX se integra una interfaz de software especializado que proporciona la precisión de la hipertermia en las coordenadas reales del objetivo.
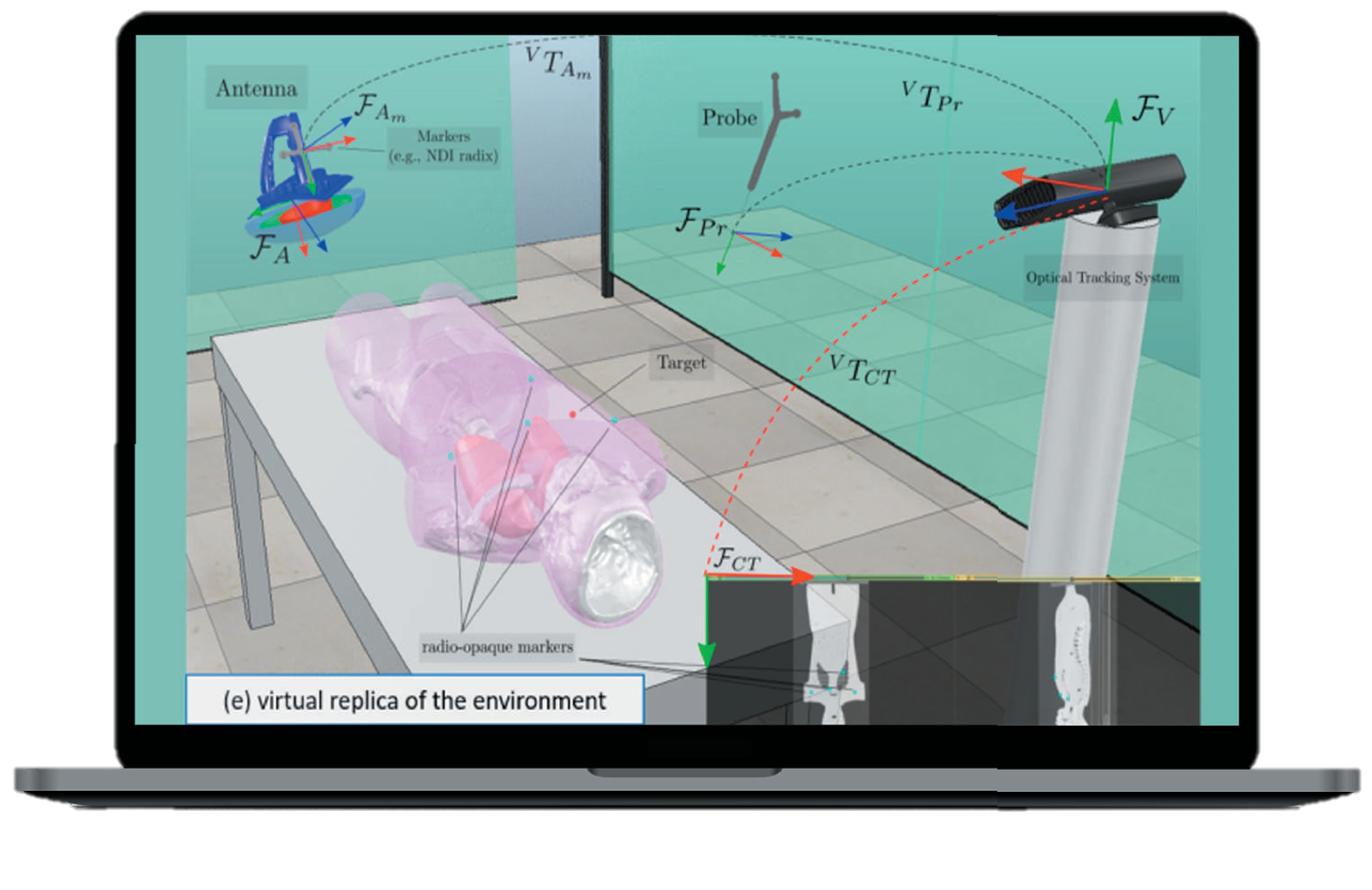
Este software de OPTIX se diseñó con el fin de reconstruir en 3D las imágenes TC del paciente, el registro virtual/real, la adquisición y visualización de la antena, el seguimiento en tiempo real de los aplicadores (ALFA, BETA, GAMMA y DELTA) y la visualización de errores de posicionamiento. Por tanto, consigue la colimación óptima del patrón SAR de las antenas. Además, proporciona dosimetría de alta calidad gracias a la alta resolución y exactitud de posicionamiento de los sensores de temperatura en la superficie tratada.
3. Impartición del tratamiento: termometría y comodidad del paciente
Dentro de la impartición de la hipertermia se considera la termometría, como monitorización de la dosis térmica que se administra, y la seguridad y comodidad del paciente dado que son tratamientos largos.
Termometría
Como ocurre en radioterapia con las UH, en hipertermia oncológica debe asegurarse que se alcanzan las temperaturas deseadas en el objetivo. Esa es la función de la termometría en vivo, prescrita en las directrices de control de calidad de la hipertermia locorregional[14].
Registrar la temperatura en el volumen objetivo o tejidos circundantes es esencial para monitorizar la calidad de la hipertermia. De esta manera, la termometría asegura una impartición efectiva, llevando un registro cuantificable de todo el tratamiento. Con la información se puede determinar la eficacia de la metodología.
Por otra parte, la termometría permite una intervención directa, ajustando parámetros ante los cambios de temperatura por sensaciones del paciente, movimientos indeseados de las sondas, perfusión de los tejidos, etc. De hecho, la perfusión es un mecanismo muy eficiente a la hora de regular la temperatura corporal y sin la monitorización en tiempo real no se puede gestionar.
Diversos estudios clínicos informan de la posibilidad de calentar tumores voluminosos con los sistemas capacitivos. Reportan que las temperaturas en el tumor están en el intervalo terapéutico (40–44 °C)[15]–[18]. Sin embargo, las medidas provienen de un número limitado de sondas que no proporcionan información completa sobre la distribución 3D de temperatura. Según van Rhoon et al.[19], no permiten detectar puntos calientes que podrían conllevar quemaduras subcutáneas[5]. A pesar de todo esto, en la actualidad la tecnología capacitiva no tiene integrado ningún sistema de termometría en sus equipos.
La tecnología radiativa cuenta con dos aproximaciones de termometría: las sondas superficiales o mínimamente invasivas de temperatura (Med-Logix) y la termometría no invasiva por resonancia magnética (Pyrexar).
La sonda de temperatura es el enfoque más convencional, directo, reproducible y preciso. Las de Med-Logix son compatibles con fuertes campos electromagnéticos. Su colocación en el cuerpo es inocua. Se distribuyen en varios puntos clave, tanto superficiales como en los de impartición, mediante las cavidades naturales o por catéter en las intersticiales. Realizan medidas frecuentes (en directo) y cualquier sensor de temperatura puede cruzarse con un patrón de referencia.

Para la hipertermia profunda, la planificación de los sensores puede hacerse con imagen guiada por medio de easyPLAN. Med-Logix ha desarrollado para ALBA 4D un sistema de dosimetría en tiempo real a través de la medición de temperatura con 64 sensores. Estos se agrupan en sondas multipunta que se colocan en las cavidades naturales del cuerpo (intracavitaria) de forma que monitoricen la temperatura durante el tratamiento en el volumen objetivo y el tejido sano. Disponen de sondas para colon, ovario, recto, cérvix, ano y vagina. Además, Med-Logix cuenta con catéteres para vejiga, esófago, páncreas y próstata.
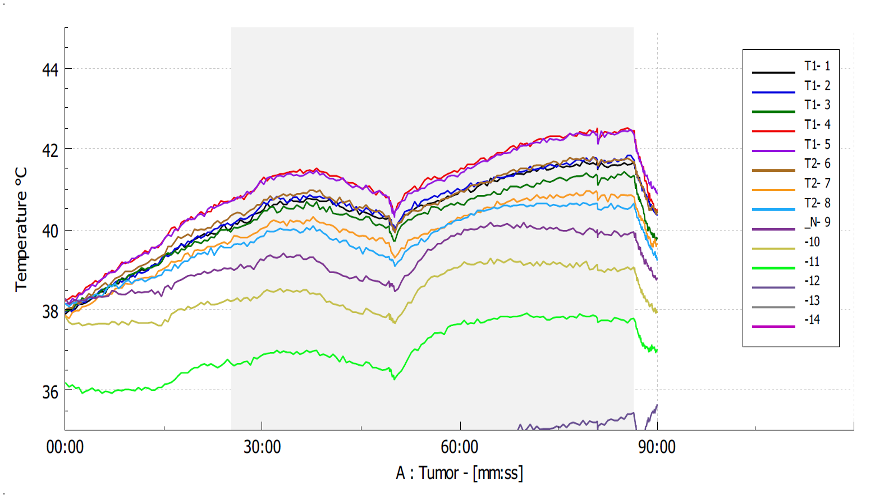
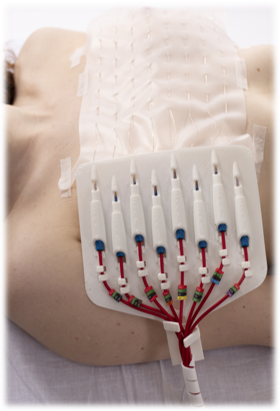
En hipertermia superficial, los sensores se colocan sobre la piel, dando un valor que puede servir de referencia de la temperatura que se está alcanzando en el tumor. ALBA ON 4000D incluye un sistema termométrico, ALBA T-Matrix, compuesto de termómetro digital de 64 canales y sábana ultraligera con una matriz de hasta 64 sensores de temperatura[22]. El número de sensores es ocho veces más alto que el mínimo recomendado por la ESHO[7], [23].
Así, detecta de modo simultáneo hasta 64 puntos espaciales en tiempo real, realizando un extenso mapeo térmico. Los datos se muestran a través de un mapa térmico que se superpone al GTV/PTV con una dosimetría más fiable del GTV/PTV. Además, el posicionamiento de las sondas es fácil y rápido [24].
Con respecto a la termometría por resonancia magnética, permite medir en directo la T1 y T2 de los tejidos durante el tratamiento. Al relacionarse con la temperatura, esta se puede conocer de forma no invasiva. El montaje es más aparatoso y complejo porque requiere del equipo de hipertermia y del de resonancia magnética. Asimismo, son medidas indirectas y, por tanto, muy dependientes de la metodología, la resolución y no es fácil contar con referencia patrón. Además, el tiempo de refresco para visualizar un mapa 3D de la temperatura según la resonancia magnética no es tan inmediato como la medida directa de las sondas. En cambio, sí proporcionaría medidas termométricas inferidas de todos los puntos de la imagen de resonancia magnética.
La termometría por resonancia magnética del abdomen sigue siendo un reto por los artefactos introducidos con el movimiento de los intestinos y heterogeneidades[20]. Por eso, las directrices de control de calidad prescriben que se requieren de forma adicional sondas de temperatura[14], [21].
Comodidad del paciente
La comunicación constante con el paciente durante el tratamiento de hipertermia posibilita adaptar la configuración de fase y potencia según su feedback. En el caso de Med-Logix, se puede utilizar el mapa de temperatura simulada de PLAN2heat, ya que proporciona información importante asociada a los puntos calientes y fríos.
Med-Logix prioriza la comodidad y seguridad del paciente en sus sistemas ergonómicos de hipertermia oncológica.
ALBA 4D cuenta con un gantry patentado adaptativo. ALBA 4D ajusta la configuración mecánica a los diferentes tamaños y anatomías del paciente gracias al movimiento monitorizado de gantry y antenas. Asimismo, los bolus adaptativos de agua que se colocan entre el paciente y el array de antenas son de diferentes tamaños (desde S a XL). De esta manera se evita la presión del agua sobre el paciente, se enfría el tejido superficial durante el tratamiento y se consigue la óptima adaptación de las antenas que asegura el depósito máximo de potencia en la región objetivo.
Por otra parte, la mesa de ALBA 4D permite su extracción rápida e integra un sistema termométrico que facilita la experiencia de usuario. Los colchones se han diseñado de forma que ofrezcan la mayor comodidad al paciente y la obtención de imágenes de TC/RM que reproduzcan con exactitud la posición durante el tratamiento.
Además, ALBA 4D es el único equipo que incluye un sistema de ventilación cuya intensidad y dirección pueden ajustarse para asegurar la comodidad del paciente. ALBA 4D también dispone de un soporte de dispositivos multimedia fácil de usar con el que se puede ver una película o escuchar música durante el tratamiento.
En ALBA ON 4000D, los aplicadores son ligeros, tienen integrado el bolus de agua y presentan una curvatura con la que se adaptan a la forma de las regiones anatómicas a tratar. Los tres ejes de rotación y tres grados de libertad permiten el posicionamiento fino del aplicador según la estructura morfológica de la anatomía del paciente. De esta forma, adapta la configuración mecánica, mejorando la eficiencia del tratamiento, la comodidad del paciente y la ergonomía para los operadores.
El enfoque adoptado por Med-Logix con sus sistemas ALBA, ALBA 4D de hipertermia profunda y ALBA ON 4000D de hipertermia superficial y semiprofunda, aproxima al máximo el flujo de trabajo a la radioterapia, de acuerdo con las directrices de la ESHO. Las distintas herramientas desarrolladas por este fabricante se dirigen a la planificación del tratamiento a partir de las imágenes de TC con el cálculo de la dosis térmica (PLAN2heat), la configuración y posicionamiento precisos (software easyPLAN y guía óptica OPTIX), la termometría con sondas durante la impartición del tratamiento y la comodidad del paciente por medio de distintas soluciones. De esta manera, lo que se pretende es seguir el modelo de flujo de trabajo efectivo de la radioterapia que garantice la hipertermia oncológica de máxima calidad.
En el próximo artículo de esta serie abordaremos la evidencia clínica de cómo la calidad del tratamiento de hipertermia con la temperatura alcanzada en el tumor es imprescindible para su efectividad clínica. Mientras tanto, puede profundizar en el flujo de trabajo de la hipertermia oncológica con el webinar bajo demanda realizado en colaboración con la SEFM.
Además, desde Aplicaciones Tecnológicas participaremos el próximo 17 de abril a las 16:00 horas en la mesa redonda sobre retos clínicos de hipertermia oncológica de la Sociedad Española de Física Médica (SEFM) con la intervención de Pablo Bellido. Las plazas para esta sesión son limitadas, por lo que recomendamos reservar la suya cuanto antes en el siguiente enlace.
Le invitamos a suscribirse a la newsletter bimestral para recibir aviso de la siguiente publicación de esta serie de Hipertermia oncológica: ¿cuál es el camino hacia el tratamiento de calidad? Puede contactarnos en el siguiente enlace.
Referencias
[1] J. van der Zee, Z. Vujaskovic, M. Kondo, and T. Sugahara, ‘The Kadota Fund International Forum 2004-Clinical group consensus’, Int. J. Hyperthermia, vol. 24, no. 2, pp. 111–122, 2008.
[2] A. Bakker et al., ‘Post-operative re-irradiation with hyperthermia in locoregional breast cancer recurrence: Temperature matters’, Radiother. Oncol., vol. 167, pp. 149–157, 2022.
[3] C. M. van Leeuwen et al., ‘A short time interval between radiotherapy and hyperthermia reduces in-field recurrence and mortality in women with advanced cervical cancer’, Radiat. Oncol., vol. 12, no. 75, 2017.
[4] H. P. Kok, F. Navarro, L. Strigari, M. Cavagnaro, and J. Crezee, ‘Locoregional hyperthermia of deep-seated tumours applied with capacitive and radiative systems: a simulation study’, Int. J. Hyperthermia, vol. 34, no. 6, pp. 714–730, Aug. 2018.
[5] H. P. Kok and J. Crezee, ‘A comparison of the heating characteristics of capacitive and radiative superficial hyperthermia’, Int. J. Hyperthermia, vol. 33, no. 4, pp. 378–386, May 2017.
[6] H. D. Trefná et al., ‘Quality assurance guidelines for superficial hyperthermia clinical trials: I. Clinical requirements’, Int. J. Hyperthermia, vol. 33, no. 4, pp. 471–482, 2017.
[7] H. Trefná Dobšíček et al., ‘Quality assurance guidelines for superficial hyperthermia clinical trials II. Technical requirements for heating devices’, Strahlenther. Onkol., vol. 193, pp. 351–366, 2017.
[8] G. Bruggmoser et al., ‘Guideline for the clinical application, documentation and analysis studies for regional deep hyperthermia’, Strahlenther. Onkol., vol. 188, no. SUPPL. 2, pp. 198–211, 2012.
[9] G. Bruggmoser, ‘Some aspects of quality management in deep regional hyperthermia’, Int. J. Hyperthermia, vol. 28, no. 6, pp. 562–569, Aug. 2012.
[10] J. J. W. Lagendijk et al., ‘ESHO quality assurance guidelines for regional hyperthermia’, Int. J. Hyperthermia, vol. 14, no. 2, pp. 125–133, 1998.
[11] H. P. Kok et al., ‘Treatment planning facilitates clinical decision making for hyperthermia treatments’, Int. J. Hyperthermia, vol. 38, no. 1, pp. 532–551, Jan. 2021.
[12] H. P. Kok and J. Crezee, ‘Hyperthermia Treatment Planning: Clinical Application and Ongoing Developments’, IEEE Journal of Electromagnetics, RF and Microwaves in Medicine and Biology, vol. 5, no. 3, pp. 214–222, 2021.
[13] J. Ödén, K. Eriksson, B. Pavoni, H. Crezee, and H. P. Kok, ‘A novel framework for thermoradiotherapy treatment planning’, Int. J. Radiat. Oncol. Biol. Phys., Feb. 2024.
[14] G. Bruggmoser et al., ‘Quality Assurance for Clinical Studies in Regional Deep Hyperthermia’, Strahlenther und Onkologie, vol. 187, pp. 605–610, 2011.
[15] M. Abe et al., ‘Multi-institutional studies on hyperthermia using an 8-MHz radiofrequency capacitive heating device (Thermotron RF-8) in combination with radiation for cancer therapy’, Cancer, vol. 58, no. 8, pp. 1589–1595, Oct. 1986.
[16] S. Masunaga et al., ‘Clinical results of thermoradiotherapy for locally advanced and/or recurrent breast cancer-comparison of results with radiotherapy alone’, Int. J. Hyperthermia, vol. 6, no. 3, pp. 487–497, 1990.
[17] N. G. Huilgol, S. Gupta, and R. Dixit, ‘Chemoradiation with hyperthermia in the treatment of head and neck cancer’, Int. J. Hyperthermia, vol. 26, no. 1, pp. 21–25, Feb. 2010.
[18] G. Li et al., ‘Local hyperthermia combined with external irradiation for regional recurrent breast carcinoma’, Int. J. Clin. Oncol., vol. 9, no. 3, pp. 179–183, June 2004.
[19] G. C. van Rhoon, J. van der Zee, M. P. Broekmeyer-Reurink, A. G. Visser, and H. S. Reinhold, ‘Radiofrequency capacitive heating of deep-seated tumours using pre-cooling of the subcutaneous tissues: results on thermometry in Dutch patients’, Int. J. Hyperthermia, vol. 8, no. 6, pp. 843–854, Nov. 1992.
[20] L. Winter et al., ‘Magnetic resonance thermometry: Methodology, pitfalls and practical solutions’, Int. J. Hyperthermia, vol. 32, no. 1, pp. 63–75, 2016.
[21] H. P. Kok et al., ‘Locoregional peritoneal hyperthermia to enhance the effectiveness of chemotherapy in patients with peritoneal carcinomatosis: a simulation study comparing different locoregional heating systems’, Int. J. Hyperthermia, vol. 37, no. 1, pp. 76–88, 2020.
[22] A. Bakker et al., ‘Two high-resolution thermal monitoring sheets for clinical superficial hyperthermia’, Phys. Med. Biol., vol. 65, no. 17, p. 175021, June 2020.
[23] A. Bakker et al., ‘Analysis of clinical data to determine the minimum number of sensors required for adequate skin temperature monitoring of superficial hyperthermia treatments’, Int. J. Hyperthermia, vol. 34, no. 7, pp. 910–917, Nov. 2018.
[24] A. Bakker et al., ‘Clinical Feasibility of a High-Resolution Thermal Monitoring Sheet for Superficial Hyperthermia in Breast Cancer Patients’, Cancers , vol. 12, no. 3644, Dec. 2020.